MIT
Zakwaszanie oceanów nie będzie problemem. Dawno temu, gdy w atmosferze było wielokrotnie więcej CO2, jak na przykład w Mezozoiku, życie w oceanach kwitło. Pomyślcie o amonitach, koralach, belemnitach, kokolitach i bogactwie innych gatunków, zamieszkujących ówczesne bardziej kwasowe wody oceanów. Nawet więc jeśli stężenie CO2 osiągnie ówczesny poziom, to życie w oceanach będzie mieć się znakomicie.
STANOWISKO NAUKI
Obecne błyskawiczne zakwaszanie się oceanu polega nie tylko na wzroście koncentracji jonów wodorowych (spadku wskaźnika pH) ale też anionów HCO3– kosztem CO32-. To właśnie niedobór tych ostatnich ma niszczący wpływ na skorupiaki i rafy koralowe.

Temat zakwaszenia oceanów – drugiego, obok globalnego ocieplenia, problemu powodowanego przez wzrost koncentracji CO2 w atmosferze – coraz częściej przewija się w mediach i negocjacjach międzynarodowych. Podobnie jak w przypadku ocieplenia klimatu pojawiły się także osoby podważające zagrożenia związane z zakwaszeniem w mniej lub bardziej uzasadniony sposób. I tak jak w przypadku globalnego ocieplenia, często wykorzystują one złożoność problemu do zaciemniania obrazu.
Co i jak się zmienia w wodzie?
Najczęściej – zgodnie ze standardami chemii – zakwaszenie oceanu opisuje się jako spadek pH, czyli wielkości, która (w dużym uproszczeniu) informuje o stężeniu jonów wodorowych H+. Wartości pH poniżej 7 to odczyn kwaśny (dużo jonów H+), a powyżej – zasadowy (mało jonów H+). Od czasów przedprzemysłowych średnie pH wody oceanicznej spadło o ok. 0,1, z ok. 8,2 do 8,1. Jak zauważy bystry obserwator, oznacza to, że woda wciąż jest zasadowa. Zmianę tę jednak nazywamy zakwaszeniem, podobnie jak zmianę temperatury powietrza z 35 na 30°C nazywamy ochłodzeniem (chociaż 30°C to wciąż bardzo ciepło). Warto ponadto zauważyć, że 0,1 wydaje się niewielką liczbą, jednak skala kwasowości jest skalą logarytmiczną – zmiana współczynnika pH o 1 odpowiada aż 10-krotnej zmianie ilości jonów wodorowych, tak więc zmiana pH o 0,1 przekłada się na wzrost ilości jonów wodorowych o blisko 30%!
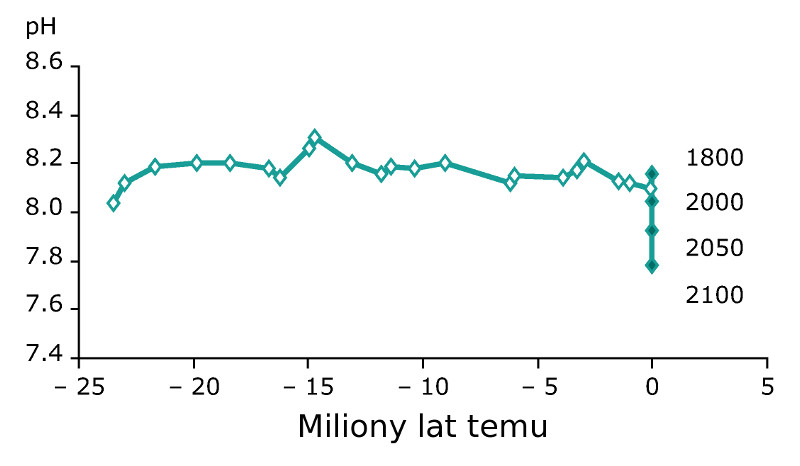
Co więcej, historia zapisana w morskich osadach pokazuje, że jest to zmiana, jakiej światowy ocean nie widział od dawna. Już teraz średni współczynnik pH wód oceanicznych spadł do poziomu najniższego od ponad 20 milionów lat.
Dlaczego wprowadzenie do wody dwutlenku węgla (CO2) skutkuje pojawieniem się w niej jonów wodorowych? Dwutlenek węgla reaguje z wodą, tworząc kwas węglowy. Kwas węglowy zaś nie trzyma się stale formy „zamkniętych” cząsteczek H2CO3, część cząsteczek dysocjuje do postaci jonów wodorowęglanowych (HCO3−) i wodorowych (H+):
CO2 + H2O <–> H2CO3 <–> HCO3− + H+
Wolne jony wodorowe są także przyłączane do unoszących się w wodzie jonów węglanowych (CO32-), przez co one również „zamieniają się” w jony wodorowęglanowe:
CO32− + 2 H+ <–> HCO3− + H+
Podkreślmy: wprowadzanie do wody CO2 prowadzi do powstania wolnych jonów H+, które z kolei eliminują z roztworu jony CO32- .I to właśnie spadek dostępności jonów węglanowych (Raport Royal Society, 2005), a nie wzrost ilości jonów wodorowych stanowi problem dla morskiego życia.
W zapisach reakcji stosujemy strzałki skierowane jednocześnie w dwie strony. Wszystkie one bowiem mogą jednocześnie zachodzić „w jedną” i „w drugą stronę” (jedne jony się łączą, inne dzielą…), tworząc stan pewnej równowagi. Warunki środowiskowe mogą jednak powodować, że któraś ze stron reakcji zostaje uprzywilejowana i zaczyna zachodzić częściej, ze zwiększonym prawdopodobieństwem.
Skały, woda i skorupki
Aby rozbudowywać swoje skorupki i szkieleciki, morskie stworzenia, takie jak małże, ślimaki czy koralowce, absorbują unoszące się w wodzie morskiej jony wapniowe (Ca2+) i węglanowe (CO32-), pochodzące między innymi z chemicznego wietrzenia skał (pamiętacie z lekcji geografii opowieści o procesach krasowych w górach Świętokrzyskich?).
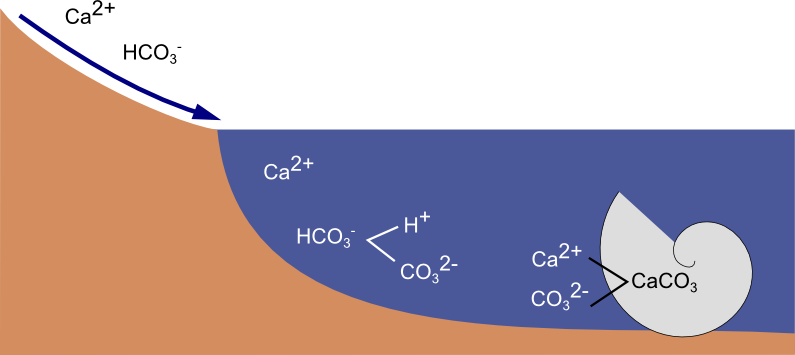
I teraz jest już jasne, czemu zamiana jonów węglanowych na wodorowęglanowe jest dla morskich stworzeń niekorzystna. Oznacza to po prostu usunięcie części potrzebnych im klocków. Wniosek ten potwierdziła seria eksperymentów opisanych w opublikowanej niedawno pracy Waldbusser i in. (2014).
Na ogół rozpuszczanie dwutlenku węgla w wodzie morskiej symuluje się w laboratorium poprzez wtłaczanie do wody bąbelków CO2. Przy takim podejściu w wodzie jednocześnie zmieniają się zawartość CO2, jonów węglanowych oraz pH. Uniemożliwia to dokładną analizę każdego z tych czynników z osobna. Waldbusser i in. (2014) zastosowali bardziej złożoną metodę przygotowania wody, w której umieszczali badane organizmy. Zaczęli od wytworzenia neutralnej „wody podstawowej”: przefiltrowaną wodę morską zobojętnili chlorowodorem oraz „wyczyścili” z węgla, pompując przez nią tlen. Następnie skomponowali 16 roztworów – dla czterech stężeń CO2 oraz czterech poziomów nasycenia wody jonami węglanowymi. Zawartość węgla w roztworach kontrolowano poprzez domieszki węglanu i wodorowęglanu sodu (Na2CO3, NaHCO3), a kwasowość z użyciem chlorowodoru (HCl). Przeprowadzono po dwa zestawy eksperymentów dla dwóch gatunków małży.
Eksperymenty pokazały, że z wyjątkiem skrajnych warunków, rozwój małż w niewielkim stopniu zależy od pH wody czy ciśnienia parcjalnego CO2 (rysunek 4 a, b). Udowodniono natomiast, że niezwykle istotnym czynnikiem jest nasycenie środowiska węglanami. Zgodnie z intuicją, im jest ich więcej, tym więcej żyjątek rozwija się prawidłowo (rysunek 4 c, d).

Oczywiście specjalnie zaprojektowane doświadczenia Waldbussera i kolegów nie oddają idealnie tego, co aktualnie obserwujemy w morskich ekosystemach. W rzeczywistości mamy obecnie do czynienia z jednoczesnymi zmianami w pH i stężeniach węglanów. W przeszłości jednak dynamika zmian koncentracji CO2, stężenia węglanów w wodzie morskiej i pH była inna, a zmiany tych parametrów nie zawsze szły ramię w ramię. Wszystko dlatego, że zmiany tych parametrów miewały różne przyczyny, oraz, że ich tempo dyktowały procesy o różnych skalach czasowych. Przykładowo, gdy wzrost koncentracji CO2 postępował powoli, to jego odkładanie się w oceanie było skutecznie ograniczane dzięki „zużywaniu” go na wspomniane wyżej wietrzenie skał (nasilające się wraz ze wzrostem temperatury). Mechanizm ten ma jednak „kiepski refleks” – działa na przestrzeni setek tysięcy i milionów lat, nie jest więc w stanie ochronić naszego oceanu, gdy my w ponad tysiąckrotnie krótszym czasie wypuszczamy do niego cały zmagazynowany głęboko pod ziemią węgiel.
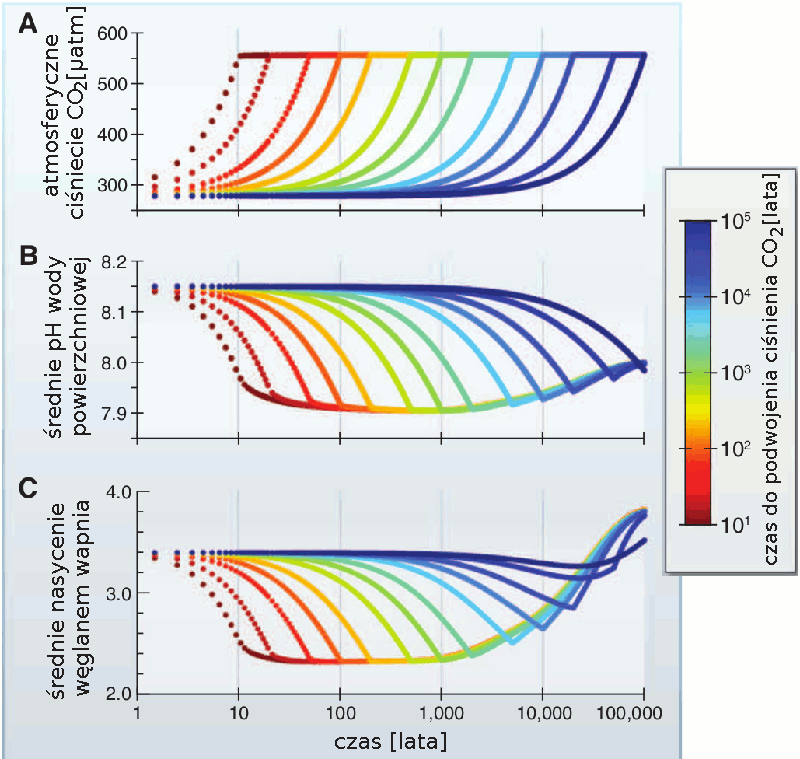
Skale czasowe, w jakich chemia oceanu reaguje na zmiany w koncentracji dwutlenku węgla w powietrzu, badano w eksperymencie numerycznym opisanym w artykule Honischa i in. (2012) (patrz rysunek 6). Użyto w nim zaawansowanego modelu środowiska ziemskiego, uwzględniającego zjawiska zachodzące w atmosferze, oceanie, na powierzchni lądów, oddziaływanie wody i lodu morskiego, procesy biochemiczne itd. (GENIE). Obliczenia wykazały, że podwojenie stężenia CO2 (z przedprzemysłowych 278 ppm do 556 ppm, niezależnie od tego ile czasu zajmuje (rys. 6A), powoduje istotny spadek pH (rys. 6B). Tymczasem nasycenie wody jonami węglanowymi nie spada znacząco tylko wtedy, gdy zmiany koncentracji CO2 zachodzą bardzo powoli (rys. 6C). Jeśli stężenie CO2 wzrasta gwałtownie (jak obecnie), to koncentracja jonów węglanowych gwałtownie spada. Koniec końców, niezależnie od tempa zmian zawartości dwutlenku węgla w atmosferze, po czasie rzędu 100 000 lat są one kompensowane przez wietrzenie skał.
„Doświadczalną” ilustrację tego zjawiska prezentuje rysunek 6. Przedstawiono na nim skamieliny glonów tego samego rodzaju pochodzące z okresu wysokich koncentracji CO2 w powietrzu, a więc i niskiego pH wody morskiej. Skamieniałość po lewej pochodzi z okresu, w którym ocean nie cierpiał na niedobór jonów węglanowych. Egzemplarz po prawej pochodzi zaś z okresu Paleo-Eoceńskiego Maksimum Termicznego (PETM, 55-56 milionów lat temu), kiedy to nagły (w skali geologicznej – ale i tak wielokrotnie wolniejszy od obecnego) wzrost koncentracji CO2 w atmosferze spowodował spadek stężenia jonów węglanowych w oceanie i erodowanie delikatnych egzoszkieletów wapiennych. (Penman i in., 2014)

Jak widać, chociaż wydaje się, że sama zmiana pH wody morskiej nie ma wielkiego wpływu na koralowce czy małże, to zupełnie inaczej jest z towarzyszącą jej zmianą nasycenia wody węglanami.
Podsumowanie
W przeszłości geologicznej Ziemi były okresy, kiedy stężenie CO2 sięgało tysięcy ppm, a życie w wodach oceanów miało się dobrze – było w nich bowiem rozpuszczonych dość jonów węglanowych, by zwierzęta miały z czego budować swoje muszle i szkieleciki. Jeśli dodatkowo CO2 było wprowadzane do oceanów powoli, to naturalne procesy miały dość czasu, by uzupełniać niedobór jonów węglanowych. Jeśli jednak zmiany atmosferycznego stężenia CO2 są zbyt szybkie, wzrost stężenia jonów H+ prowadzi do drastycznego spadku stężenia jonów CO32-. W skrajnych warunkach może to prowadzić nawet do “wyciągania” ich ze skorupek. Chemicznie rzecz biorąc, jest to ten sam proces, jaki rozgrywa się podczas wietrzenia skał osadowych (które przecież właśnie z takich skorupek powstały…). Osłabienie i niszczenie tych drobnych organizmów ma poważne konsekwencje dla łańcucha pokarmowego.
Aleksandra Kardaś na podstawie Waldbusser i in. (2014), Skeptical Science [1] , Skeptical Science [2] i Ocean portal, konsultacja merytoryczna: prof. Jan M. Węsławski
Fajnie, że tu jesteś. Mamy nadzieję, że nasz artykuł pomógł Ci poszerzyć lub ugruntować wiedzę.
Nie wiem, czy wiesz, ale naukaoklimacie.pl to projekt non-profit. Tworzymy go my, czyli ludzie, którzy chcą dzielić się wiedzą i pomagać w zrozumieniu zmian klimatu. Taki projekt to dla nas duża radość i satysfakcja. Ale też regularne koszty. Jeśli chcesz pomóc w utrzymaniu i rozwoju strony, przekaż nam darowiznę w dowolnej wysokości






