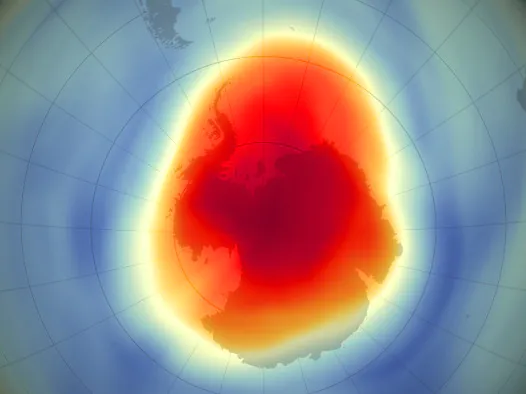
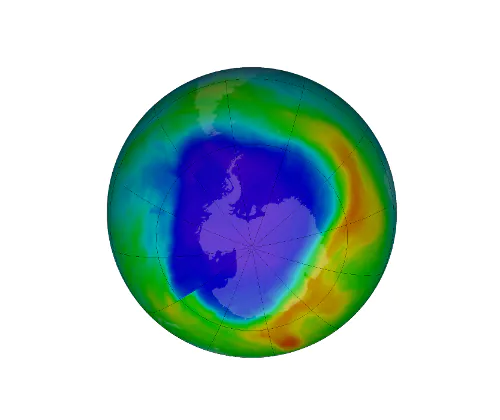
Dziura ozonowa to problem, o którym głośno było w latach osiemdziesiątych i na początku dziewięćdziesiątych XX wieku. Osoby po trzydziestce na pewno pamiętają liczne doniesienia na temat szkodliwości dezodorantów w sprayu, czynnika chłodniczego w lodówkach i wizje zagrożenia ze strony promieniowania ultrafioletowego. Zapadło nam to w pamięć do tego stopnia, że do dziś wiele osób pyta: „A co się stało z dziurą ozonową? Przecież miała nas już wszystkich zabić?”. Otóż dziura wciąż istnieje, a to, że przestała rosnąć jest wielkim sukcesem nauki i społeczności międzynarodowej. Niestety w ostatnich latach pojawiło się nowe-stare zagrożenie dla warstwy ozonowej. O tym wszystkim przeczytasz w naszym artykule.
Ozon to po prostu trójatomowa cząsteczka tlenu, O3. Takie molekuły są dużo mniej stabilne niż „standardowe” cząsteczki dwuatomowe, dlatego ozonu jest w atmosferze bardzo mało. Występuje przede wszystkim w dwóch rejonach:
- przy powierzchni Ziemi, gdzie pojawia się w wyniku oddziaływania różnego rodzaju zanieczyszczeń (związków azotu produkowanych przez samochody czy związków organicznych, np. substancji czyszczących) ze światłem słonecznym,
- w stratosferze, na wysokości kilkunastu-kilkudziesięciu kilometrów, gdzie stale zachodzą reakcje tworzenia i rozbijania cząsteczek ozonu i tlenu, związane z pochłanianiem słonecznego promieniowania ultrafioletowego (UV).
Niezależnie od wysokości, jego własności fizyczne i chemiczne są oczywiście takie same – w szczególności jest to gaz cieplarniany. Mimo to my, jako ludzkość, ozon lubimy lub nie, zależnie od tego, gdzie się znajduje. W warstwie przyziemnej traktujemy go jako niepożądanego gościa, ponieważ jest silnym utleniaczem, więc jego wdychanie jest dla nas niezdrowe (np. Wolfe i Patz, 2002, McKee, 1993), a w dodatku stanowi zagrożenie dla uprawianych przez nas roślin (np. Krupa i Manning, 1988, McKee, 1993, Ainsworth i in. 2012). Z kolei jego obecność w stratosferze jest dla nas niezwykle cenna – tu nie może nam bezpośrednio zaszkodzić, tworzy natomiast warstwę chroniącą nas przed promieniowaniem ultrafioletowym, którego nadmiar uszkadzałby nasze tkanki (np. Norval i in., 2011, 2007, de Gruijl i in., 2003).
Ozonowa [nie]równowaga
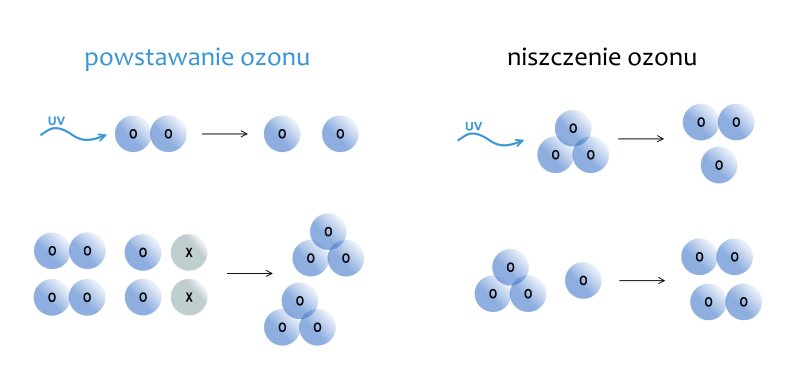
Molekuły „dobrego ozonu” w stratosferze nieustannie ulegają rozpadom – to właśnie w tym procesie pochłaniane jest promieniowanie ultrafioletowe (rysunek 2). Proces ten nie niepokoiłby nas, gdyby jednocześnie tyle samo cząsteczek ozonu powstawało. Okazuje się jednak, że istnieją mechanizmy, dzięki którym rozpady ozonu robią się częstsze, bardziej prawdopodobne (i niekoniecznie wymagają UV). Ich występowanie prowadzi do zachwiania równowagi pomiędzy tworzeniem i niszczeniem ozonu, co w skrajnym przypadku powoduje powstawanie „dziury” w warstwie ozonowej.
Jak odkryto w latach siedemdziesiątych (Molina i Rowland, 1974, Molina, 1996), w „podkradaniu” ozonu mogą brać udział związki chemiczne produkowane przez człowieka, „freony”. Ściśle rzecz biorąc, są to chloro-fluoropochodne węglowodorów, czyli związki powstające, gdy w metanie (CH4), etanie (C2H6) czy propanie (C3H8) zamienimy atomy wodoru (H) na atomy chloru (Cl) lub fluoru (F). Są one bardzo trwałe, niepalne i nieszkodliwe dla człowieka, a jednocześnie łatwo jest je skraplać i odparowywać. Dlatego znalazły wiele zastosowań, na przykład w chłodnictwie czy jako gazy nośne dla produktów sprzedawanych w puszkach aerozolowych (np. dezodoranty).
Jak się okazało, ich trwałość ma też swoje wady: gdy dostaną się do atmosfery, pozostają w niej bardzo długo i mają szansę rozpaść się dopiero wtedy, gdy niesione ruchami powietrza wywędrują w górne rejony warstwy ozonowej. Dostępne tu promieniowanie ultrafioletowe rozbija ich wiązania i powoduje uwalnianie atomów chloru. Oswobodzone atomy chloru mogą z kolei wchodzić w rekcje z cząsteczkami ozonu, „zabierając” im atomy tlenu. Co więcej, jeden atom chloru może zniszczyć wiele cząsteczek ozonu (zobacz reakcje na rysunku 3).

Cykl niszczenia ozonu zostaje przerwany dopiero, gdy atomy chloru wejdą w reakcje z innymi związkami. Niestety zachodzą także reakcje, które z powrotem wprowadzają chlor (w postaci jonów Cl– lub ClO–) do gry. O skomplikowanej chemii stratosferycznej przeczytasz na przykład w artykułach McElroy i in. (1986), Molina i Molina (1987), Abatt i Molina, (1993), Solomon (1999).
Prawdopodobieństwo poszczególnych reakcji prowadzących do niszczenia ozonu czy uwalniania atomów chloru lub jonów ClO– zależy od panujących w atmosferze warunków. Istotne są w szczególności temperatura i dostępności powierzchni, na których mogłyby te reakcje zachodzić. To dlatego znaczących ubytków ozonu nie obserwujemy na całym świecie, a tylko w konkretnych lokalizacjach i porach roku: w okolicach biegunów (południowego – regularnie, północnego – sporadycznie), pod koniec nocy polarnej. To właśnie tu i wtedy możliwe jest powstawanie w stratosferze chmur – tak zwanych „polarnych chmur stratosferycznych” (ang. polar stratospheric clouds, PSC). Są one rzadkim zjawiskiem, ponieważ w stratosferze (w przeciwieństwie do niższych warstw atmosfery) znajduje się mało pary wodnej. Dopiero gdy temperatura spada poniżej -78°C, w powietrzu pojawiają się kropelki kwasu siarkowego i azotowego*, a przy temperaturze poniżej -83°C kryształki lodu (np. Browell i in. 1990, Molina i in. 1993, Peter 1997). Na powierzchni tych cząstek dochodzi do reakcji, w których powstają jony ClO–, których obecność umożliwia kolejne cykle reakcji niszczących ozon. W rezultacie powstaje i rozrasta się dziura ozonowa (Molina i in. 1993, Solomon 1999, Voigt i in. 2000, Harris i in. 2010).

Powstawaniu chmur stratosferycznych sprzyjać mogą duże erupcje wulkaniczne, podczas których w wyższe partie atmosfery dostają się związki siarki tworzące następnie kropelki kwasu siarkowego (Stoiber i Jepsen 1973, Solomon i in. 1996, Klobas i in. 2017). Efekty z tym związane są jednak złożone: w środkowej stratosferze niszczenie ozonu spowalnia a w dolnej – przyśpiesza. To, który proces „wygrywa” zależy od wielu czynników, przede wszystkim dostępności freonów. Najnowsze analizy wskazują, że gdy ich koncentracje spadną, erupcje wulkaniczne mogą zacząć sprzyjać tworzeniu, a nie niszczeniu ozonu (Klobas i in. 2017).
Wreszcie dziura ozonowa
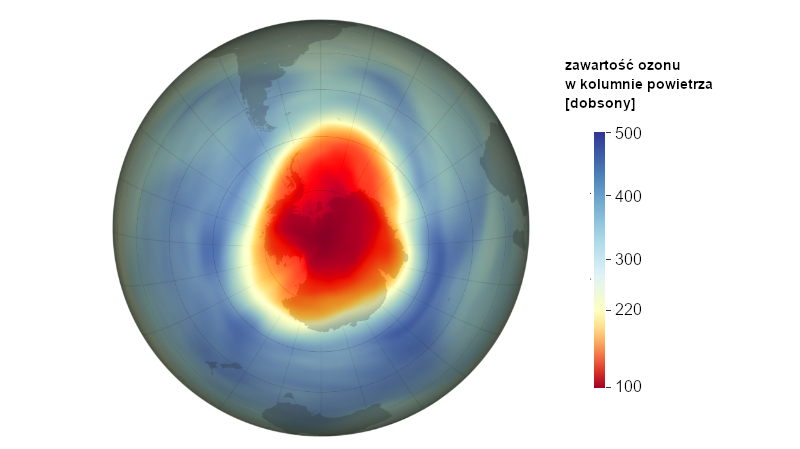
Warstwa ozonowa nie przypomina obrusa – nie jest jednolitą warstwą, w której cząsteczki ozonu przylegałyby do siebie. To otaczająca Ziemię otoczka o grubości kilkunastu kilometrów, w której luźno poruszają się cząsteczki ozonu i pozostałe gazy tworzące atmosferę. Aby określić, ile ozonu znajduje się w sumie w kolumnie powietrza, podaje się, jak grubą warstwę utworzyłby, gdyby wyciągnąć go z atmosfery i umieścić na powierzchni Ziemi (w tak zwanych warunkach standardowych, czyli ciśnieniu 1000 hPa i temperaturze 0°C). Wynik podany w metrach byłby niezwykle mały, mnożymy go więc przez 100 000 i w ten sposób otrzymujemy grubość warstwy w specjalnej jednostce nazwanej na cześć jednego z pierwszych badaczy warstwy ozonowej, G.M.B. Dobsona – dobsonem (ang. Dobson Unit, DU).
Średnia grubość warstwy ozonowej to zaledwie 300 dobsonów (3 mm), obszar, w którym spadnie ona poniżej 220 DU nazywamy dziurą ozonową. Kryterium to zostało przyjęte ze względu na fakt, że przed rokiem 1979 tak niskie zawartości ozonu były rzadkością, natomiast po roku 1979 zaczęły one być regularnie obserwowane (Newman i in. 2004). Należy pamiętać, że jest to próg umowny. Nawet jeśli nie zostaje on osiągnięty, to ryzyko chorób związanych ze zwiększoną ekspozycją na UV i tak rośnie wraz z obniżeniem koncentracji ozonu (np. Norval i in., 2011, 2007, de Gruijl i in., 2003).
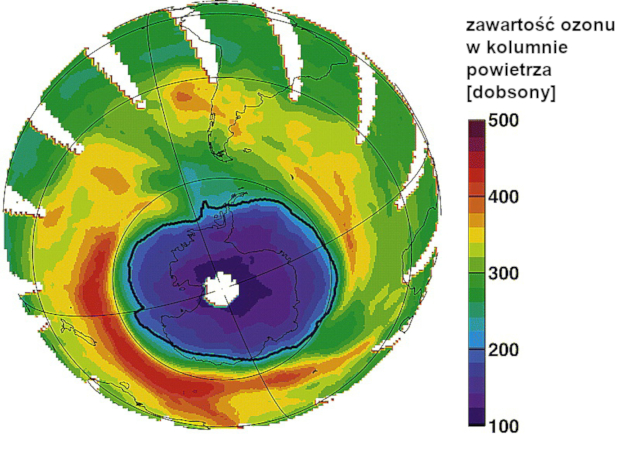
Chociaż naukowcy zaczęli obawiać się o los ozonu stratosferycznego już w latach siedemdziesiątych (Johnston, 1971, Molina i Rowland, 1974), problem spotkał się z szerszym zainteresowaniem dopiero w latach osiemdziesiątych, gdy obserwacje potwierdziły występowanie nad Antarktydą dramatycznie obniżonych (w porównaniu z dotychczasową historią pomiarów) koncentracji ozonu (Farman i in. 1985).
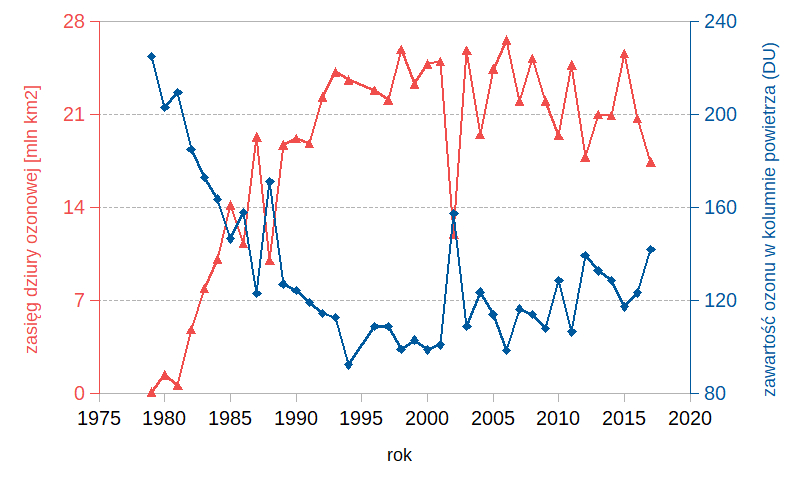
Jak pokazały pomiary, dziura ozonowa pojawia się tu cyklicznie: podczas zimy polarnej na powierzchni cząstek tworzących chmury stratosferycznych dochodzi do licznych reakcji tworzących jony ClO–, a pojawienie się pierwszych promieni Słońca uruchamia uwalnianie swobodnych atomów chloru, jak opisaliśmy to wcześniej (Solomon 1999). W rezultacie największe ubytki ozonu są na półkuli południowej obserwowane na przełomie września i października (początek tamtejszej wiosny). Najmniejszą koncentrację ozonu zaobserwowano tu w roku 1994 – średnia w dniach 21.09-16.10 wyniosła zaledwie 92 dobsony. Największy zasięg dziury ozonowej przypadł z kolei na rok 2006, w dniach 7.09-13.10 wynosił on średnio 27 mln km2 (dane za stroną NASA Ozone Watch).
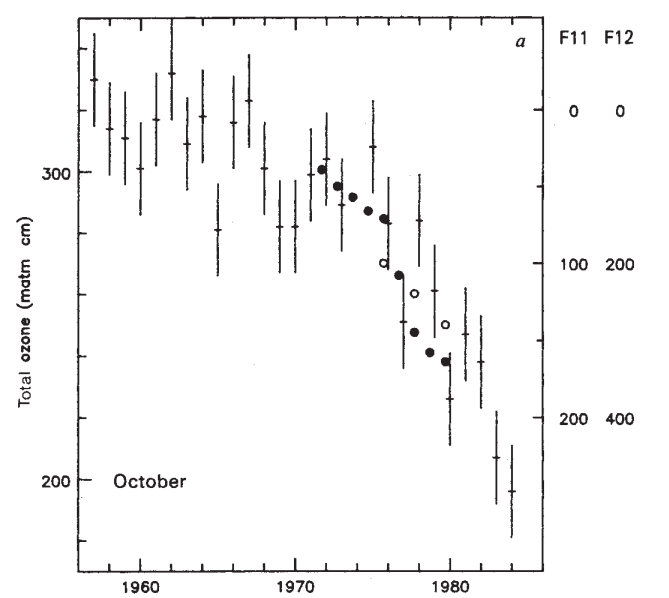
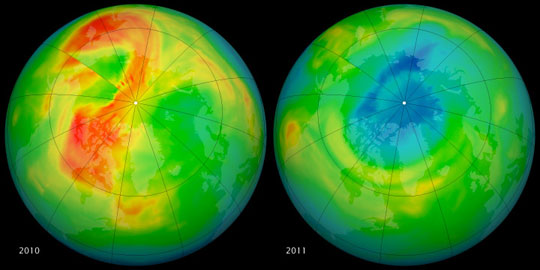
Temperatury w stratosferze nad Arktyką są zwykle wyższe niż nad Antarktyką, co skutkuje rzadszym występowaniem chmur stratosferycznych i mniejszym zagrożeniem dla warstwy ozonowej. Jednak również tu obserwuje się okresy obniżonej koncentracji ozonu. W marcu 2011, po wyjątkowo długim okresie dużego obniżenia temperatury w stratosferze i powstaniu w niej silnego wiru „ściągającego” cząsteczki zanieczyszczeń, po raz pierwszy doszło do epizodu zakwalifikowanego jako pojawienie się dziury ozonowej na półkuli północnej (Manney i in. 2011). Zawartość ozonu w kolumnie powietrza spadła wtedy o 38%. Znaczne obniżenie koncentracji ozonu w Arktyce (o 27%) nastąpiło także zimą 2015-2016, tym razem jednak nie zarejestrowano koncentracji ozonu rzędu lub poniżej 220 DU (Pommereau i in. 2018).
Wielkie cerowanie
W związku z rosnącą liczbą dowodów na niszczący wpływ freonów na warstwę ozonową i obawami o przyszłość warstwy ozonowej, chroniącej nas przed niebezpiecznym promieniowaniem ultrafioletowym (m.in. Molina i Rowland 1974, Farman i in. 1985, Solomon i in. 1986, WMO 1988), państwa zrzeszone w Organizacji Narodów Zjednoczonych uchwaliły w roku 1985 Konwencję Wiedeńską o ochronie warstwy ozonowej, a w 1987 tzw. Protokół montrealski. Dokumenty zostały ratyfikowane przez wszystkie kraje świata, które tym samym zobowiązały się do stopniowego wycofania z produkcji substancji niszczących ozon, przede wszystkim freonów. Postanowienia protokołu były kilkukrotnie poprawiane, by ostatecznie zapewnić spadek koncentracji szkodliwych substancji w atmosferze w XXI wieku (patrz rysunek 8).
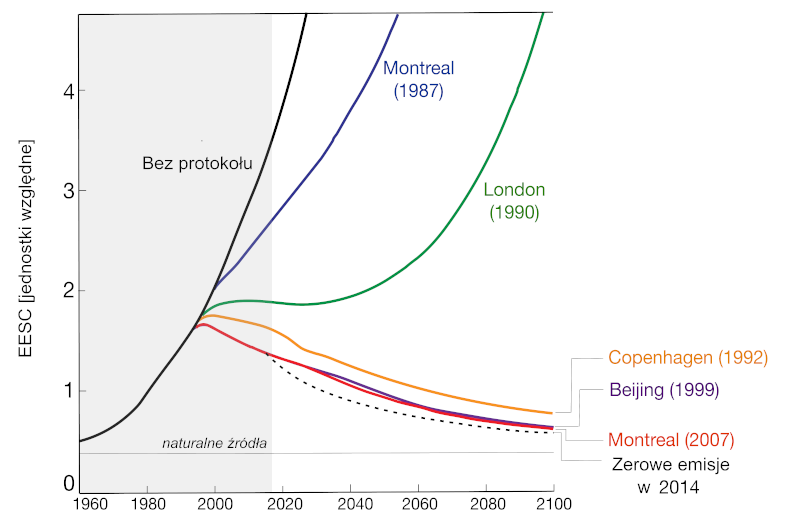
Przy okazji warto zauważyć, że Protokół montrealski znacząco zmniejszył także zagrożenie związane ze zmianą klimatu, ponieważ freony są silnymi gazami cieplarnianymi i gdyby ich dodawanie do atmosfery nie zostało zahamowane, mielibyśmy dziś do czynienia z dużo silniejszym efektem cieplarnianym, co szczegółowo opisujemy w osobnym artykule Przed czym uchronił nas Protokół montrealski. Najnowsza poprawka do Protokołu, uchwalona w 2016 r. w Kigali (weszła w życie na początku roku 2019) dotyczyła już nie substancji niszczących ozon, ale używanych w ich zastępstwie HFC – hydrofluorowęglowodorów (Bolaji i in. 2011, Wallington i in. 1995), które podobnie jak CFC mogą istotnie nasilić efekt cieplarniany i przyśpieszyć ocieplanie się klimatu (Pinnock i in. 1995, Zhang i in. 2011).
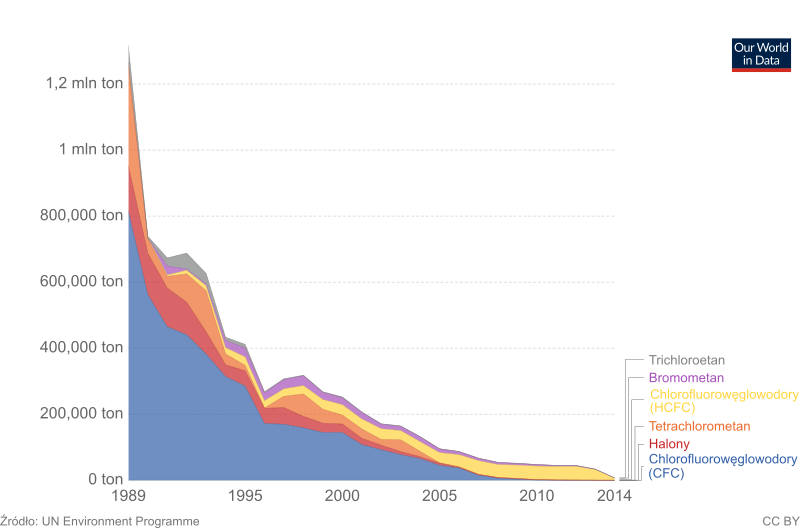
Rysunek 9 pokazuje, jak z biegiem lat zmieniało się zużycie substancji objętych Protokołem montrealskim. Ponieważ czas życia freonów w atmosferze jest bardzo długi, nikt nie oczekiwał, że zaprzestanie ich wykorzystania spowoduje ich natychmiastowe zniknięcie z atmosfery. Jak pokazuje rysunek 8, spodziewamy się powolnego, trwającego kilkadziesiąt lat spadku ich wpływu na ozon. W połowie XXI wieku sytuacja powinna wrócić do stanu z lat osiemdziesiątych XX wieku. Pojawiły się już pierwsze opracowania wykazujące, że warstwa ozonowa zaczęła się z wolna odbudowywać oraz wiążące ten fakt z malejącymi koncentracjami substancji niszczących ozon (Shepherd i in. 2014, Solomon i in. 2016, Strahan i Douglass 2018) – patrz rysunek 10.
Nie wszystko idzie gładko
Niestety jest jednak za wcześnie, by ogłosić „happy end”. Jak w prawdziwym horrorze, gdzie ostatnia scena sugeruje, że „wroga” nie udało się jeszcze do końca wyeliminować i będzie o czym nakręcić drugą część.
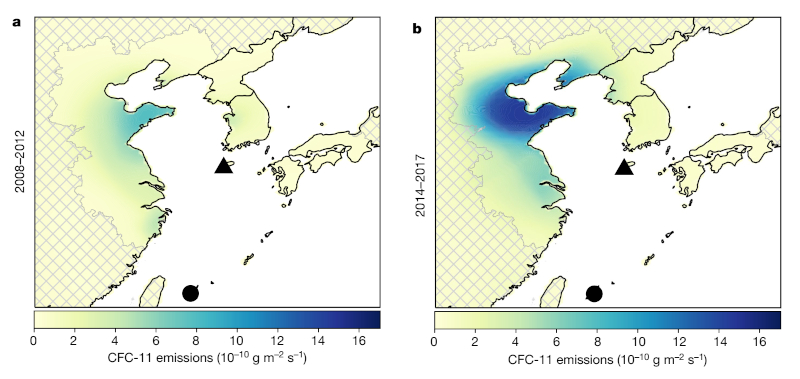
W roku 2018 ukazał się w Nature artykuł Montzki i kolegów (2018), w którym wykazano, że chociaż po roku 2012 nikt nie przyznawał się do produkcji CFC-11 (trichlorofluorometanu), a jego koncentracja w atmosferze wciąż spadała, to jednak zaczęła spadać o połowę wolniej niż wcześniej. Na podstawie pomiarów i obliczeń ustalono, że przyczyną jest nielegalna, niezgłoszona do specjalnego Sekretariatu ds. Ozonu Programu Środowiskowego ONZ produkcja tego związku.

W 2019 Rigby i in. potwierdzili na podstawie pomiarów atmosferycznych to, co już wcześniej sugerowały wyniki śledztw dziennikarskich i prowadzonych przez organizacje pozarządowe (Buckley i Fountain, 2018, EIA 2018): nowe emisje CFC-11 pochodzą z Chin, przede wszystkim z prowincji Szantung. Dokumentacja zebrana przez dziennikarzy Buckley i Fountain, 2018 wskazuje, że w substancje niszczące ozon (jako stosunkowo tanie i mające dobre parametry użytkowe) wciąż są tam wykorzystywane przy produkcji pianek poliuretanowych znajdujących zastosowanie w izolacji urządzeń chłodniczych oraz budynków. Władze chińskie deklarują, że prowadzą działania zmierzające do wykrycia odpowiedzialnych za zanieczyszczenie fabryk i usunięcia nieprawidłowości.
Sukces nauki
To, jak poradziliśmy sobie z wytworzonym przez nas zagrożeniem dla warstwy ozonowej to prawdziwa historia sukcesu. Ostrzeżeni przez naukowców politycy zgodzili się na wspólne działanie, a sprawnie wprowadzone regulacje pozwoliły na uniknięcie katastrofy i zahamowanie wzrostu dziury ozonowej.
Ostatnie doniesienia o nowych emisjach CFC-11 pokazują, że choć monitoring postępów w realizacji traktatów takich jak Protokół montrealski opiera się w dużej mierze na deklaracjach państw-stron, to nawet jeśli ktoś świadomie dostarczałby nieprawdziwych danych o emisjach, fałszerstwo zostanie wykryte. Podobne narzędzia – stałe naziemne i satelitarne pomiary składu atmosfery oraz zachodzących w niej zjawisk – pomogą nam także w weryfikacji tego, jak poszczególne kraje wypełniają zobowiązania do zmniejszenia emisji gazów cieplarnianych, jakie nałożyły na siebie w związku z Porozumieniem Paryskim (por. np. Kort i in., 2014 oraz Satelitarne obserwacje stężeń, źródeł emisji i miejsc pochłaniania CO2).
Aleksandra Kardaś, konsultacja merytoryczna: prof. Szymon P. Malinowski
—————————————
* Związki siarki dostają się do atmosfery na przykład w efekcie erupcji wulkanicznych (np. Stoiber i Jepsen 1973, Stoiber i in. 1987), a azotu są emitowane m.in. przez bakterie glebowe (Crutzen, 1970, Bates i Hays, 1967) i silniki, np. samolotów (Johnston, 1971).
Fajnie, że tu jesteś. Mamy nadzieję, że nasz artykuł pomógł Ci poszerzyć lub ugruntować wiedzę.
Nie wiem, czy wiesz, ale naukaoklimacie.pl to projekt non-profit. Tworzymy go my, czyli ludzie, którzy chcą dzielić się wiedzą i pomagać w zrozumieniu zmian klimatu. Taki projekt to dla nas duża radość i satysfakcja. Ale też regularne koszty. Jeśli chcesz pomóc w utrzymaniu i rozwoju strony, przekaż nam darowiznę w dowolnej wysokości