W poprzednim odcinku naszego cyklu zajęliśmy się wykorzystaniem izotopów węgla do odtwarzania historycznych koncentracji CO2 oraz ustalania jego pochodzenia (Paleoklimatologia: co nam powie skład izotopowy węgla). Dziś pora na izotopy tlenu. Na naszą szczególną uwagę zasługują klasyczny, „lekki” 16O z ośmioma neutronami w jądrze, oraz bardziej masywny 18O, który tych neutronów ma aż 10.
Cykl artykułów o metodach paleoklimatologii:
Paleoklimatologia: o co w tym w ogóle chodzi?
Co nam powie skład izotopowy węgla
Izotopy tlenu a temperatura
Aktywność słoneczna i radioaktywne izotopy
Sekrety rdzeni lodowych
CO2 – jeśli nie rdzenie lodowe, to co?
Drzewa, korale i stalaktyty
Tempo zachodzenia reakcji chemicznych zależy od rodzaju izotopów, jakie biorą w niej udział. Te cięższe reagują wolniej, ponieważ są mniej ruchliwe i rzadziej wchodzą w kontakt z innymi substratami niż ich szybsi lżejsi kuzyni. To, na ile uprzywilejowane są lżejsze izotopy, zależy od temperatury, w której zachodzi reakcja – izotopowy skład „produktu” stanowi więc użyteczny paleotermometr (czyli wskaźnik temperatury w przeszłości).

Wyzwanie mogą tu stanowić zmiany składu izotopowego środowiska, w którym zachodzi reakcja, a które same mogą być związane ze zróżnicowanym zachowaniem izotopów. Przykładowo, w przypadku korzystania z izotopów tlenu jako paleotermometru musimy wziąć pod uwagę zmiany rozmiaru lądolodów. Dlaczego? Prześledźmy, skąd bierze się tworzący je lód.
Wędrówka wody: od oceanu do lądolodu
Zacząć trzeba w nieoczywistym miejscu – w oceanie rejonów podzwrotnikowych, gdzie woda intensywnie paruje z powierzchni oceanu. „Zwykła” cząsteczka wody składa się z dwóch lekkich izotopów wodoru 1H i jednego lekkiego izotopu tlenu 16O (czyli ma wzór H216O), ale w cząsteczce wody mogą też występować cięższe izotopy tworząc HD16O i H218O (D oznacza deuter, czyli ciężki wodór 2H). Molekuły zawierające lekkie izotopy mają średnio wyższą średnią prędkość (co wynika z tego, że w danej temperaturze różne molekuły mają taką samą średnią energię kinetyczną), wyparowują więc łatwiej, niż cząsteczki zawierające cięższe izotopy. W powstającej w niskich szerokościach geograficznych parze wodnej występuje więc względna nadwyżka cząsteczek wody z lekkimi izotopami.
W wodzie, z której parowanie jest intensywne, stosunek liczby molekuł z atomami 18O do tych z 16O będzie wyższy niż w wodzie, z której parowanie jest słabsze. Intensywne parowanie prowadzi do wzrostu zasolenia wody, więc woda o wyższym stosunku 18O/16O jest bardziej słona niż woda o niższym stosunku 18O/16O. Samo zasolenie wód powierzchniowych (od którego zależy gęstość jonów w wodzie) także wpływa na parowanie i stosunki izotopów tlenu, co stanowi poważny i nie do końca rozwiązany problem przy interpretacji paleotemperatur powierzchni oceanu, dlatego zalecane jest, w miarę możności, jednoczesne użycie kilku paleotermometrów równocześnie.

W miarę przemieszczania się do góry oraz w stronę biegunów, powietrze ochładza się, a zawarta w nim para wodna kondensuje, tworząc chmury, a z czasem także opady. Ponieważ cząsteczki wody z ciężkimi izotopami łatwiej ulegają skropleniu (wolniejsze molekuły łatwiej się ze sobą łączą), krople deszczu (lub płatki śniegu) szybciej usuwają je z powietrza – względna nadwyżka lekkich izotopów w parze wodnej rośnie więc jeszcze bardziej.
Jako, że ilość wody w atmosferze jest zupełnie pomijalna w porównaniu z ilością wody w oceanach, nie miałoby to żadnego znaczenia, gdyby nie transport wody znad oceanów nad ląd, a w szczególności powstawanie lądolodów. Woda, która w formie śniegu spada na lądolód, pozostaje w nim na długie lata: w miarę jak śnieg osiada, jest przygniatany przez kolejne warstwy opadów, nadtapia się i zamarza, tworząc pokłady lodu. I, jak wynika z naszej opowieści, lód ten jest już silnie wzbogacony w lekkie izotopy. Tym samym woda pozostająca w oceanach jest w nie zubożona, inaczej mówiąc, pojawia się więc w niej nadwyżka ciężkich izotopów, deuteru i 18O. Analizując względną zawartość izotopów tlenu i wodoru w rdzeniach lodowych i osadach oceanicznych możemy określić, jak wiele wody znajdowało się w lądolodach, co także stanowi bardzo ważną informację o klimacie naszej planety.
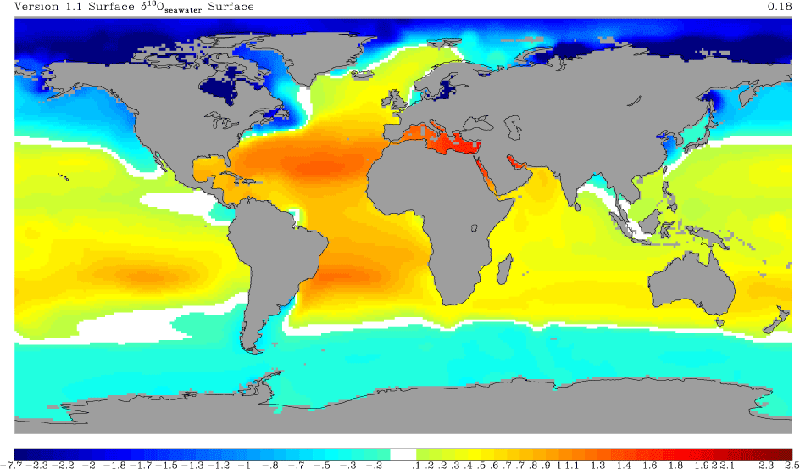
Jak opisujemy skład izotopowy próbki – wskaźnik 18O
Skład izotopowy zwykle opisujemy, wyrażając w promilach nadwyżkę/niedobór rzadziej występującego izotopu. Podobnie jak dla izotopów węgla (patrz Paleoklimatologia: co nam powie skład izotopowy węgla) dla koncentracji tlenu 18O względem 16O tworzymy wskaźnik:
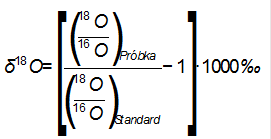
Stosunek 18O/16O w ogólnie przyjętym standardzie (tzw. Wiedeński Standard Uśrednionej Wody Oceanicznej, Vienna Standard Mean Ocean Water – VSMOW) wynosi 1/498,7.
Ujemne wartości wskaźnika oznaczają, że w próbce występuje niedobór 18O względem standardu, dodatnia wartość pokazuje zaś nadwyżkę. Przykładowo, wartość wskaźnika 18O równa -5‰ oznacza, że stosunek ilości atomów 18O do ilości atomów 16O w próbce jest mniejszy niż w standardzie, czyli Uśrednionej Wodzie Oceanicznej o 0,001•5•1/498,7, czyli 10 cząsteczek na milion (10 ppm).
W ostatnich 100 tys. lat, ilość 18O w padającym na lądolód Grenlandii śniegu zmieniała się od -42‰ podczas epok lodowych (zimno, duże lądolody, duży niedobór 18O w wodzie oceanów) do -35‰ obecnie (ciepło, mniejsze lądolody, mniejszy niedobór 18O w wodzie oceanów), a na Antarktydzie od -40‰ do -55‰ (separacja izotopów jest szczególnie intensywna w głębi Antarktydy).
Izotopy tlenu w osadach oceanicznych
Jednym ze sposobów mierzenia dawnych temperatur jest analiza składu izotopowego węglanowych pancerzyków malutkich organizmów takich jak otwornice. Muszelki otwornic są bardzo zróżnicowane, łatwo więc odróżnić i wyselekcjonować gatunki żyjące na interesującej nas głębokości toni wodnej – należące do przypowierzchniowego lub głębszego planktonu albo na dnie morskim w postaci bentosu.

W zależności od temperatury organizmy (pierwotniaki) te wbudowują w swoje zmineralizowane węglanem wapnia (CaCO3) skorupki, lekkie (16O) i cięższe (18O) izotopy tlenu w różnych proporcjach. Możemy tę zależność zmierzyć i w laboratorium: im temperatura jest wyższa, tym więcej jest lekkiego tlenu 16O względem cięższego 18O. I to jest właśnie nasz paleotermometr, który pozwala nam wykonać pomiary sięgające dziesiątki, a nawet setki milionów lat w przeszłość. Korekty uwzględniające zmiany względnej ilości izotopów tlenu w oceanach, związanej z istnieniem czap lodowcowych wykonać można dzięki pomiarom rdzeni lodowych i innym metodom. W epokach, kiedy na Ziemi nie było lądolodów tego problemu nie mamy.

Skorupki otwornic w osadach oceanicznych zachowują też inne sygnatury pozwalające na rekonstrukcję dawnego klimatu. Przykładowo, porównanie izotopowego składu węgla (znany z poprzedniego artykułu wskaźnik δ13C), wchodzącego w skład węglanowych skorupek otwornic należących do planktonu i bentosu daje nam cenne informacje o cyklu węglowym w oceanach.
Marcin Popkiewicz i Aleksandra Kardaś, konsultacja merytoryczna: dr hab. Jarosław Tyszka i inni
Fajnie, że tu jesteś. Mamy nadzieję, że nasz artykuł pomógł Ci poszerzyć lub ugruntować wiedzę.
Nie wiem, czy wiesz, ale naukaoklimacie.pl to projekt non-profit. Tworzymy go my, czyli ludzie, którzy chcą dzielić się wiedzą i pomagać w zrozumieniu zmian klimatu. Taki projekt to dla nas duża radość i satysfakcja. Ale też regularne koszty. Jeśli chcesz pomóc w utrzymaniu i rozwoju strony, przekaż nam darowiznę w dowolnej wysokości







