Gazy cieplarniane – dlaczego są cieplarniane? Jaka jest ich definicja? Co decyduje o ich własnościach?
Cykl „efekt cieplarniany dla średniozaawansowanych”:
Termiczna struktura atmosfery
Gazy cieplarniane i ich cechy
Wpływ gazów cieplarnianych na widmo promieniowania ziemskiego
Zmiany koncentracji gazów cieplarnianych a transport energii
Wpływ chmur
Aerozole
Bilans energetyczny Ziemi

Zdjęcie Marka Fergusa zamieszczamy dzięki uprzejmości CSIRO (licencja CC BY 3.0).
Bardzo ważną cechą atmosfery jest to, że jest ona niemal przezroczysta dla słonecznego promieniowania krótkofalowego i niemal nieprzezroczysta dla promieniowania długofalowego wypromieniowywanego przez powierzchnię Ziemi (patrz Efekt cieplarniany – jak to działa). To właśnie temu zjawisku zawdzięczamy istnienie efektu cieplarnianego oraz sprzyjającą rozwojowi życia temperaturę powierzchni Ziemi.
Gazy cieplarniane – gazy, które słabo lub wcale nie oddziałują z promieniowaniem słonecznym, ale pochłaniające promieniowanie podczerwone w zakresie długości fal emitowanych przez powierzchnię Ziemi (inaczej długofalowe promieniowanie ziemskie).
Przeważająca część gazów znajdujących się w ziemskiej atmosferze, w tym azot i tlen, nie pochłania ani nie emituje promieniowania długofalowego – jest więc dla niego przezroczysta. Na rysunku 2 po lewej stronie pokazane są cząsteczki gazów niepochłaniających i nieemitujących promieniowania długofalowego, po prawej zaś stronie cząsteczki gazów pochłaniających je i emitujących. Przyjrzyj się cząsteczkom z obu grup. Dostrzegasz różnicę między nimi?
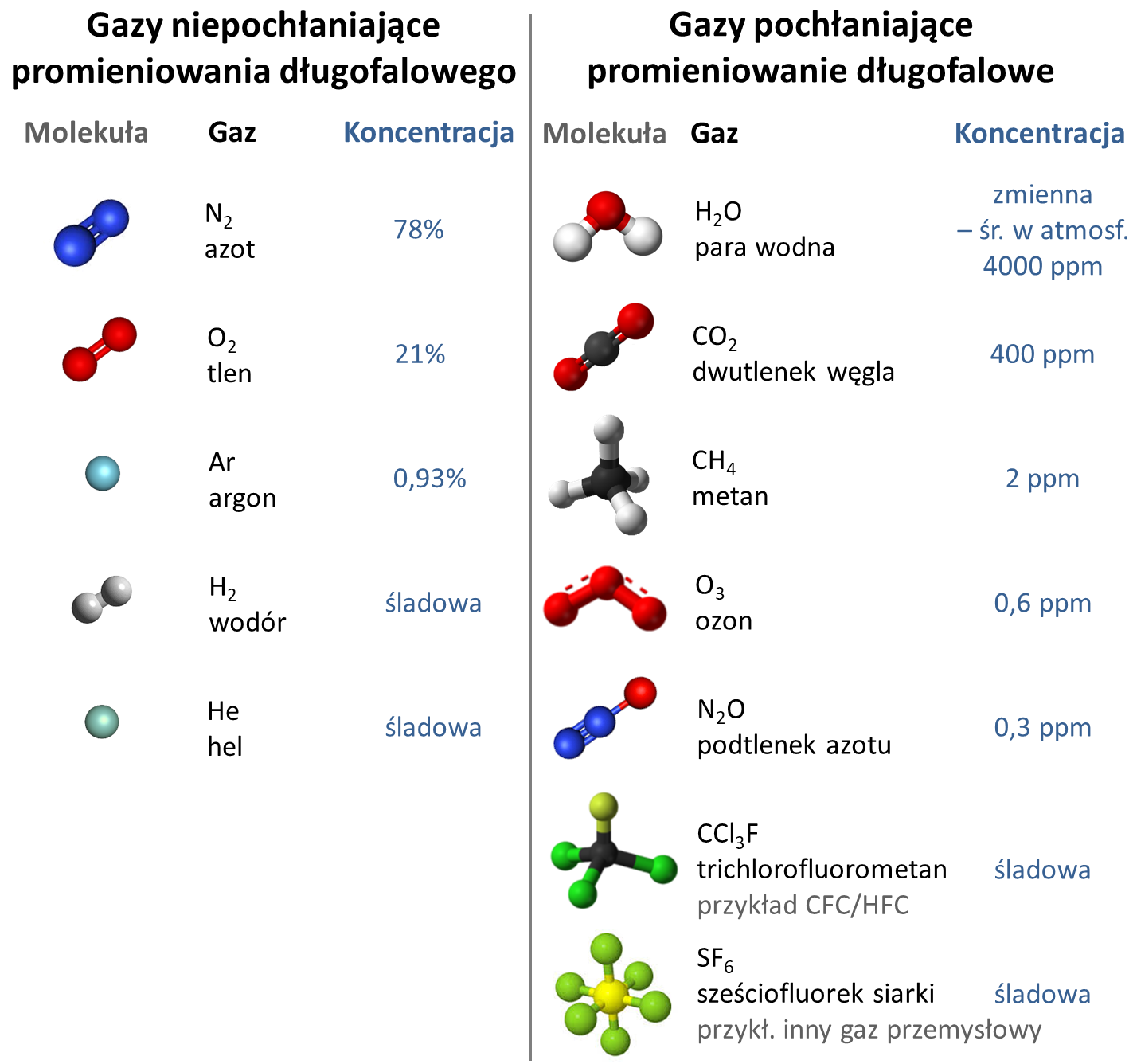
Promieniowania długofalowego nie pochłaniają i nie emitują cząsteczki składające się z dwóch identycznych atomów oraz pojedyncze atomy (atomy gazów szlachetnych, takich jak hel czy argon w ogóle nie wchodzą w reakcje chemiczne i nie tworzą cząsteczek – dlatego zresztą zyskały nazwę gazów szlachetnych).
Choć cząsteczki składające się z dwóch różnych atomów (jak np. tlenek węgla CO lub chlorowodór HCl) mają widma pozwalające na absorpcję i emisję promieniowania długofalowego, to cząsteczki te ze względu na ich wysoką reaktywność i rozpuszczalność mają bardzo krótki czas życia w atmosferze i nie przyczyniają się w znaczącym stopniu do efektu cieplarnianego – można je więc pominąć.
Znajdujące się w atmosferze cząsteczki gazów cieplarnianych składają się z trzech i więcej atomów.
Czemu to ma znaczenie? Ruchy cząsteczek a pochłanianie podczerwieni
Cząsteczki składają się z atomów, które z kolei składają się z masywnych, dodatnio naładowanych jąder atomowych oraz lekkich, ujemnie naładowanych elektronów. Najprostszy opis atomu (model Bohra) przedstawiał atomy jako masywne jądro i elektrony krążące wokół niego po swoich orbitach, podobnie jak planety wokół Słońca. Model ten nie jest jednak właściwy ze względu na dualną, korpuskularno-falową naturę elektronów. Obecnie atom przedstawiany jest więc jako skupiające praktycznie całą masę jądro, otoczone rozmytą chmurą elektronów.
Dodatnio naładowane jądra atomów zawsze się odpychają, jednak uwspólnienie elektronów przez atomy może prowadzić do korzystnej konfiguracji energetycznej – w takiej sytuacji jądra atomowe utrzymują się w pewnej odległości od siebie, tworząc cząsteczkę. Nazywamy to wiązaniem chemicznym. Można je porównać do sprężyny mającej na końcach dwa jądra atomowe, która umożliwia im pewną swobodę przybliżania się i oddalania od siebie. Takie ich drgania nazywamy oscylacjami.
Pobudzenie cząsteczek do drgań
Oscylację cząsteczki mogą pobudzić drgania pola elektrycznego związane z promieniowaniem elektromagnetycznym – o ile mają częstotliwość odpowiednią dla tego konkretnego zestawu atomów. W ten sposób energia promieniowania zostaje pochłonięta przez cząsteczkę. Mechanizm przekazywania energii jest przy tym dwustronny – z jednej strony energia może być zaabsorbowana przez cząsteczkę (oscylator), a z drugiej może też zostać z niej wyemitowana w formie promieniowania. Cząsteczka pochłania i emituje energię w tych samych długościach fal. Informację o tym, jakie długości fali pochłania i emituje wybrany związek lub mieszanina, nazywamy widmem absorpcyjno-emisyjnym.
W cząsteczkach składających się z dwóch takich samych atomów (na przykład N2 czy O2) rozkład ładunków jest symetryczny – zmiany pola elektromagnetycznego nie wzbudzają więc niesymetrycznych drgań czy obrotów pola elektrycznego takiej cząsteczki. Energia kwantów promieniowania podczerwonego jest zbyt mała, żeby wzbudzić drgania symetryczne, więc azot, tlen (i inne gazy składające się z dwóch takich samych atomów) nie pochłaniają promieniowania w tym zakresie, nie są więc gazami cieplarnianymi.
W cząsteczkach niesymetrycznych w rozkładzie ładunków występuje nierównowaga – jedna strona cząsteczki ma niewielki ładunek dodatni, druga zaś niewielki ujemny (taki układ nazywamy dipolem elektrycznym). Przykładem są molekuły wody.
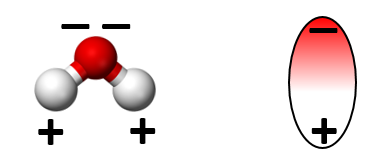
Drgania takiej cząsteczki, a także jej obracanie (rotacja), a przy cząsteczkach wieloatomowych rozciąganie i zginanie, oznaczają zmiany pola elektrycznego w ich otoczeniu. Odpowiednio, zmiany zewnętrznego pola elektrycznego wzbudzają oscylacje i rotacje cząsteczek. To, jakie drgania i obroty wykonuje cząsteczka, nazywamy jej stanem oscylacyjno-rotacyjnym. Do wzbudzenia wielu stanów oscylacyjno-rotacyjnych wystarcza stosunkowo niewielka energia kwantów promieniowania podczerwonego.
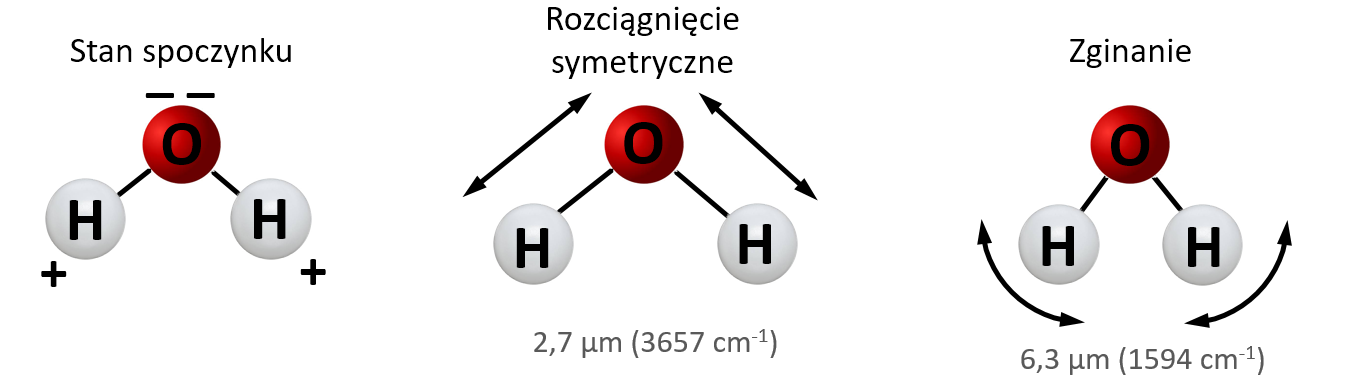
Promieniowanie podczerwone mogą też pochłaniać cząsteczki wieloatomowe nie będące dipolami (apolarne), np. molekuły CO2, które mają kształt linii prostej z atomem węgla pośrodku i dwoma atomami tlenu na obu końcach. Obrót takiej cząsteczki lub rozciąganie symetryczne nie powodują zmiany ładunku, jednak rozciąganie asymetryczne i zginanie powodują polaryzację.
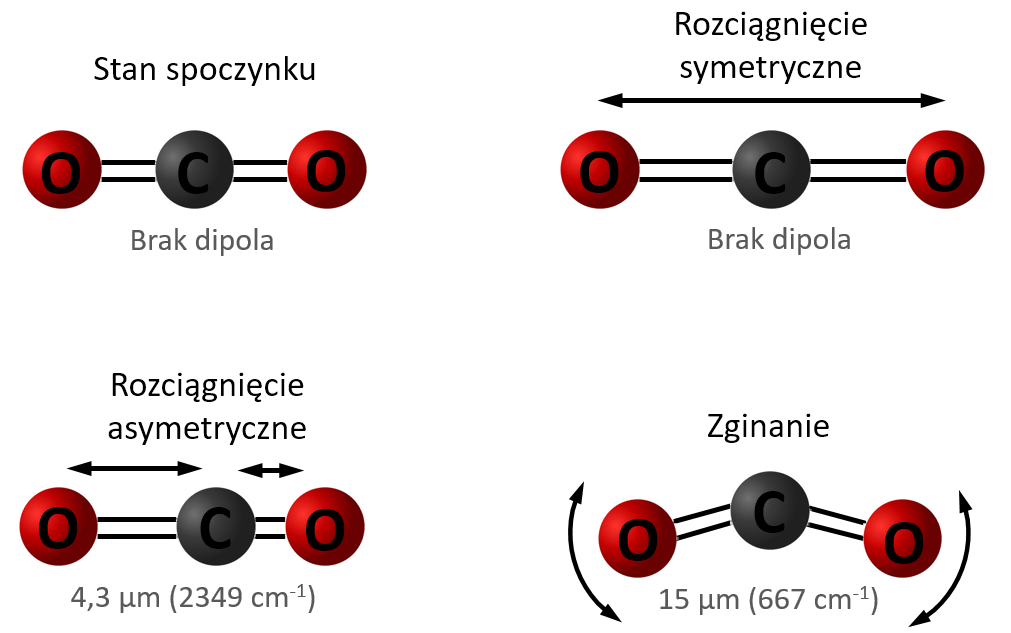
Widma absorpcyjne gazów cieplarnianych (oscylacyjno-rotacyjne)
W rezultacie nakładania się na siebie wielu różnych rodzajów rotacji i drgań cząsteczki gazów takich jak H2O czy CO2 mają wiele możliwych stanów energetycznych. Cząsteczki mogą zmieniać swój stan energetyczny, absorbując bądź emitując fotony o energii odpowiadającej różnicy energii związanych z poszczególnymi stanami. Inaczej mówiąc, cząsteczki takie mają rozbudowane widma absorpcyjno-emisyjne i oddziałują z promieniowaniem w szerokim zakresie częstotliwości. Dla podkreślenia, że absorpcja (lub emisja) promieniowania jest związana ze zmianami stanów oscylacyjno-rotacyjnych cząsteczek (a nie innymi zjawiskami zachodzącymi wewnątrz nich), używa się czasem określenia „widmo oscylacyjno-rotacyjne”. Cząsteczki gazów cieplarnianych składają się z trzech i więcej atomów, bo tylko takie cząsteczki mają widma oscylacyjno-rotacyjne pozwalające na absorpcję i emisję promieniowania podczerwonego.
Linie i pasma absorpcyjne
Z powodów historycznych mówimy o liniach spektralnych, odpowiadających długościom fali, w których jakiś ośrodek – na przykład atmosfera ziemska albo atmosfera Słońca czy innej gwiazdy – pochłania promieniowanie elektromagnetyczne. Dwutlenek węgla, który jest cząsteczką trójatomową, ma skomplikowane widmo oscylacyjno-rotacyjne składające się z tysięcy linii widmowych. W interesujących nas okolicach – czyli dla fal o długościach charakterystycznych dla promieniowania ziemskiego czy promieniowania termicznego atmosfery – wygląda ono tak:
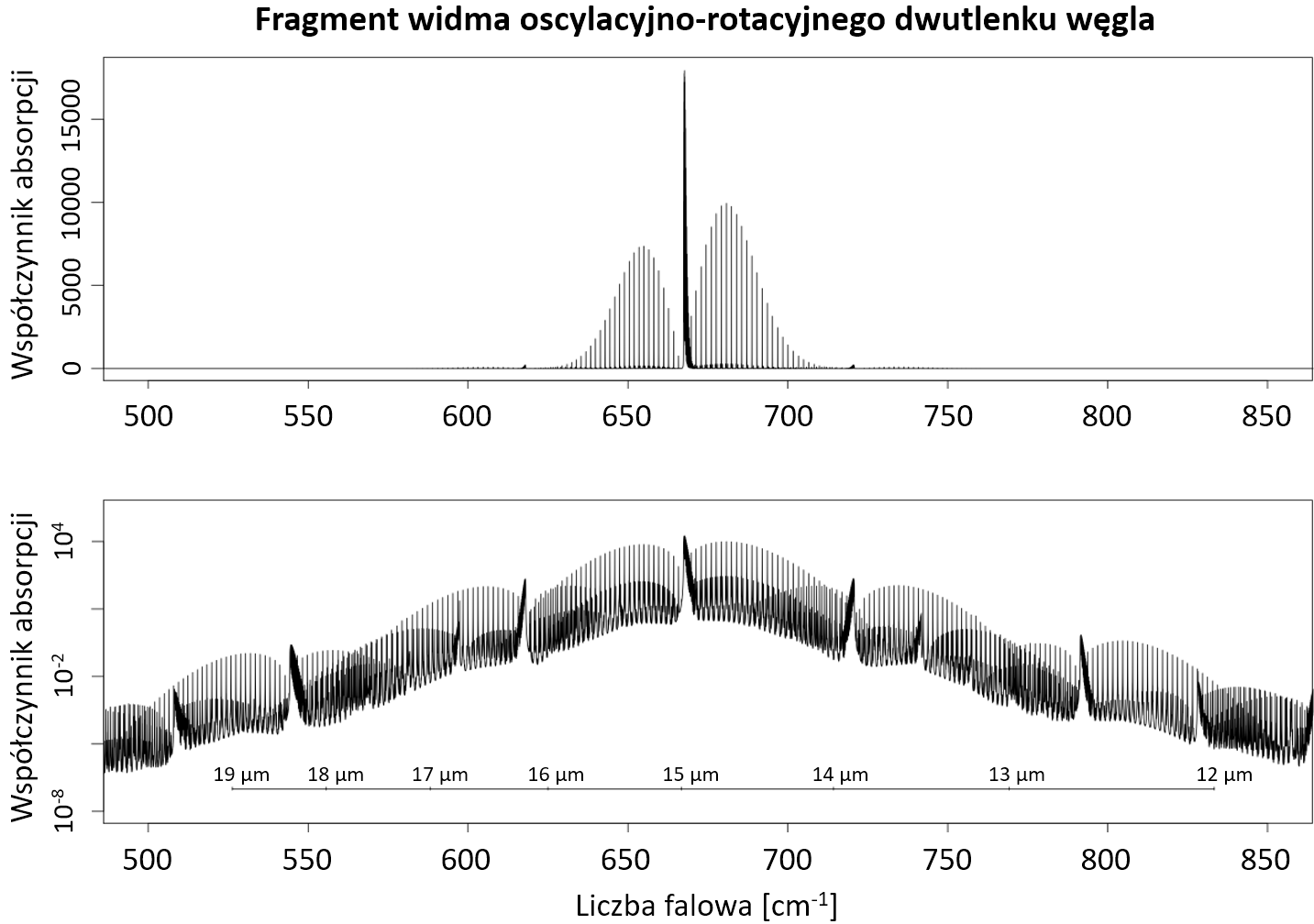
Nawet jednak taki obraz nie oddaje całej złożoności aspektów pochłaniania promieniowania. W rzeczywistości każda z linii widmowych jest „poszerzona”: molekuła może pochłonąć nie tylko fale konkretnej długości, ale też fale długości trochę mniejszej lub większej. Poszerzone linie widmowe często łączą się z innymi blisko położonymi, tak że zamiast o jednej konkretnej długości fal pochłanianych przez jakąś substancję, wygodniej jest mówić o ich zakresie. Taki zakres nazywamy pasmem absorpcji.
Poszerzenie linii widmowych – co za nie odpowiada?
Poszerzenie linii widmowych jest wynikiem współdziałania kilku zjawisk.
Po pierwsze, stan energetyczny cząsteczki (na który składają się jej energia kinetyczna związana z przemieszczaniem się, oscylacjami i rotacjami oraz energia potencjalna elektronów na powłokach atomowych), nie jest jednoznacznie określony. Gdybyśmy wzięli dużą liczbę takich samych cząsteczek i nadali im taką samą prędkość, drgania i rotacje, nie miałyby one identycznych energii, lecz leżałyby one w wąskim przedziale wartości. To jedna z sytuacji, w których znaczenie ma zasada nieoznaczoności Heisenberga, o której możesz się więcej dowiedzieć z podręcznika do mechaniki kwantowej. Dla nas jest istotne, że skoro energia cząsteczek w poszczególnych stanach nie jest jednoznacznie określona, to również różnice energii pomiędzy stanami są rozmyte (czyli są różne, choć bardzo do siebie zbliżone). To z kolei oznacza, że cząsteczki mogą emitować i pochłaniać promieniowanie z pewnego zakresu wokół linii widmowej.
Po drugie, poszczególne cząsteczki dwutlenku węgla czy pary wodnej w atmosferze, nawet jeśli oscylują i rotują w ten sam sposób, to jednocześnie poruszają się w przestrzeni w różne strony i z różnymi prędkościami, chaotycznie. Oznacza to, że dzięki efektowi Dopplera ta sama fala ma z punktu widzenia poszczególnych molekuł trochę różne długości. Oznacza to również, że nawet fala mająca długość odbiegającą trochę od „idealnej” różnicy pomiędzy stanami energetycznymi, może zostać pochłonięta – wystarczy, że trafi na cząsteczkę poruszającą się z odpowiednią prędkością. W atmosferze zjawisko to jest szczególnie istotne na dużych wysokościach, zwłaszcza w termosferze, gdzie cząsteczki miewają wystarczająco duże prędkości.
Trzecim efektem jest tak zwane „poszerzenie ciśnieniowe”. Jest ono konsekwencją zderzeń pomiędzy cząsteczkami. Zderzenia są tym bardziej prawdopodobne, im większe jest ciśnienie gazu. Pozwalają molekułom pochłaniać fotony nieidealnie dopasowane do różnicy energii pomiędzy stanami oscylacyjno-rotacyjnymi – nadmiar energii może być bowiem oddany innej cząsteczce przy okazji zderzenia. Na różnych wysokościach, na których panują różne ciśnienia, zjawisko to ma zróżnicowany wpływ – najistotniejszą rolę odgrywa ono w najniższych partiach atmosfery, gdzie panują najwyższe ciśnienia.
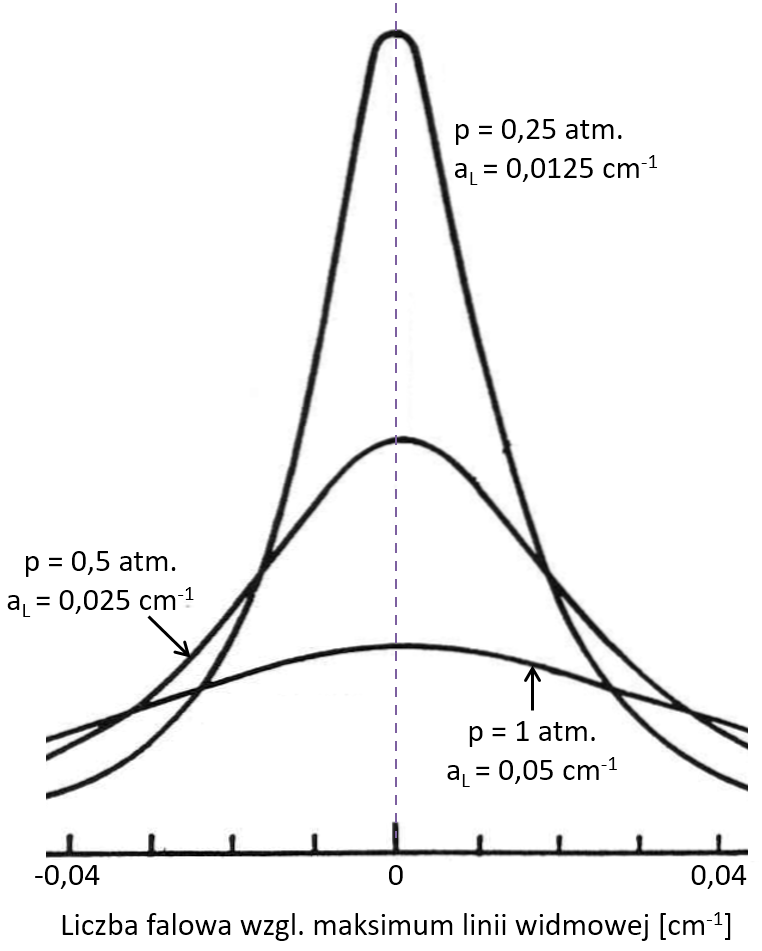
Procesy pochłaniania i emisji promieniowania są na tyle złożone, że nie da się ich opisać tak prostym wzorem jak dla modelu szyby (patrz: Efekt cieplarniany – jak to działa?). Na szczęście są to zjawiska, które stosunkowo łatwo bada się eksperymentalnie, mamy więc obszerną wiedzę na ich temat, a do prowadzenia obliczeń wykorzystać możemy komputery.
Wiecie, kto badał gazy cieplarniane?
Znaczna część naszej wiedzy o szczegółach widma absorpcyjnego CO2 i wielu innych gazów cieplarnianych pochodzi z programów badawczych zainicjowanych w czasach zimnej wojny i wyścigu zbrojeń między USA a ZSRR. Częściowo były to badania o charakterze podstawowym, ale celem niektórych było rozwiązanie problemów takich jak np. naprowadzanie pocisków przeciwlotniczych, wykrywanie startów międzykontynentalnych rakiet balistycznych czy projektowanie wysokoenergetycznych laserów zdolnych do ich niszczenia.

Skorzystała na tym fizyka atmosfery i astronomia podczerwona, bo nikt nie chciałby pomylić ataku nuklearnego z chmurami albo bombowca strategicznego z meteorem. W szczególności, powszechnie używana dzisiaj przez klimatologów, planetologów i astronomów baza linii spektralnych HITRAN, z której pochodzą dane prezentowane np. na ilustracji 6, powstała w laboratorium badawczym sił powietrznych Stanów Zjednoczonych w Hanscom.
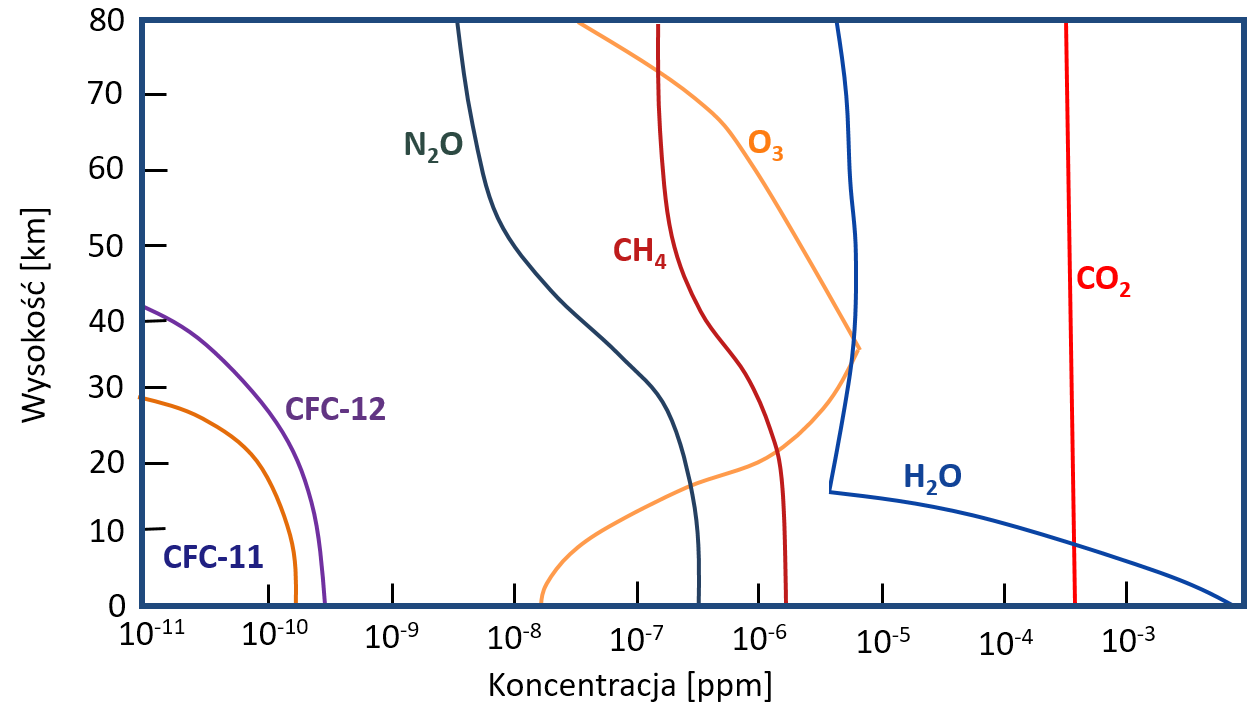
W kolejnym artykule przyjrzymy się temu, jak pochłanianie promieniowania przez gazy cieplarniane wpływa na widmo opuszczającego Ziemię promieniowania, jak zmienia ono bilans radiacyjny planety i temperaturę jej powierzchni. Aby dobrze to zrozumieć, przyda nam się jeszcze informacja o tym, gdzie w atmosferze występują poszczególne gazy.
Artykuł jest przeredagowanym na potrzeby publikacji w internecie fragmentem książki Marcina Popkiewicza, Aleksandry Kardaś i Szymona Malinowskiego pt. Nauka o klimacie.
Fajnie, że tu jesteś. Mamy nadzieję, że nasz artykuł pomógł Ci poszerzyć lub ugruntować wiedzę.
Nie wiem, czy wiesz, ale naukaoklimacie.pl to projekt non-profit. Tworzymy go my, czyli ludzie, którzy chcą dzielić się wiedzą i pomagać w zrozumieniu zmian klimatu. Taki projekt to dla nas duża radość i satysfakcja. Ale też regularne koszty. Jeśli chcesz pomóc w utrzymaniu i rozwoju strony, przekaż nam darowiznę w dowolnej wysokości







